Identifizierung der Grundursache für 'ein zunehmendes Problem'
'Eine wachsende Sorge'
Genetische Varianten des Melanocortin-4- Rezeptor(MC4R)-Signalwegs können sich auf die Regulierung von Hunger, Nahrungsaufnahme, Sättigung und Energieverbrauch auswirken.1,2
Melanocortin-4-Rezeptor und Adipositas
Eine gestörte MC4R-Signalübertragung kann unabhängig von Umwelt- und Lebensstilfaktoren zu Hyperphagie (pathologischer, unstillbarer Hunger) sowie schwerer Adipositas im Kindesalter führen.3,4
Es gibt über 113 Gene, die möglicherweise mit dem MC4R-Signalweg in Verbindung stehen, und seltene genetische Varianten innerhalb des MC4R-Signalwegs können zu einer gestörten neuronalen Signalgebung führen, die seltene genetische Erkrankungen wie Adipositas mit Proopiomelanocortin-Mangel (POMC) und Adipositas mit Leptinrezeptormangel (LEPR) verursachen kann.4,5
Nicht-diagnostizierte Grundursache
Eine der Grundursachen der schweren Adipositas im Kindesalter wird zu selten diagnostiziert. Die proaktive Identifizierung der Hauptsymptome kann dazu beitragen, dass Kinder mit einer seltenen Erkrankung des MC4R-Signalwegs richtig behandelt werden können.4,6
Sie haben eine spezielle Frage?
Wenn Sie weitergehende Fragen haben oder ein Thema ausführlicher besprechen möchten, wenden Sie sich an unser Team.Proaktives, personalisiertes Adipositas-Management
Prof. Luca Busetto spricht über die Notwendigkeit eines proaktiven Adipositas-Managements, bei dem die Grundursache der Adipositas ermittelt und eine personalisierte Behandlung durchgeführt wird.
Rhythm Pharmaceuticals is leveraging a IQVIA's Healthcare Professional Authentication solution to identify your eligibility to access this video content. If you already have an IQVIA account using it with other healthcare providers, please click 'Login' otherwise click 'Signup'.
Identifikation einer seltenen Erkrankung des MC4R- Signalwegs
Sobald die Hauptsymptome Hyperphagie und schwere Adipositas im Kindesalter erkannt werden, kann ein genetisches Screening dazu beitragen, das Vorliegen einer seltenen Erkrankung des MC4R-Signalwegs festzustellen.7
Wenn Sie erwägen, Ihre Patienten auf eine seltene Erkrankung des MC4R-Signalwegs zu untersuchen, denken Sie an die folgenden Hauptsymptome:8

Gesteigertes und länger anhaltendes Hungergefühl

Kürzere Dauer des Sättigungsgefühls

Starke gedankliche Fixierung auf das Thema Essen

Längere Dauer bis zum Erreichen des Sättigungsgefühls

Erheblicher Stress und unangemessene Reaktion bei Nahrungsverweigerung

Auffälliges essenszentriertes Verhalten (zB nächtliches Essen, Stehlen von Nahrung, Suche nach Nahrung im Müll)
Schwere Adipositas im Kindesalter (d. h. die Erkrankung tritt im typischen Fall vor dem 5. Lebensjahr auf).4,9,10
Eine BMI-Kurve, die deutlich über den Referenzperzentilen liegt, kann auf eine zugrundeliegende seltene Erkrankung des MC4R-Signalwegs hinweisen.
Informationen zur Behandlung
Die genetische Adipositas ist eine latente Bedrohung


Beschleunigung der Überweisung
Um seltene Erkrankungen des MC4R-Signalwegs frühzeitig zu erkennen, müssen einige wichtige klinische Untersuchungen durchgeführt werden:11
- Eine detaillierte Anamnese ist entscheidend
- Erfassung der Familiengeschichte, sofern verfügbar
Eine anamnestisch bekannte Resistenz gegen herkömmliche Strategien des Adipositas-Managements kann ein nützliches Kriterium für die Diagnose sein.
Zwar sind individuelle Varianten rar, doch seltene Erkrankungen des MC4R-Signalwegs sind bei Menschen mit schwerer Adipositas im Kindesalter vermutlich nicht selten. Das Patientenalter beim Auftreten der Adipositas ist ein Schlüsselfaktor bei der Erkennung von Patienten mit potenziellen Varianten in Adipositas-assoziierten Genen.4,6
01
— 03
Wissensbibliothek
Klicken Sie hier, um weitere Informationen über seltene Erkrankungen des MC4R-Signalwegs sowie von Rhythm angebotene Schulungsmaterialien und-veranstaltungen zu finden.
Wir aktualisieren diese Seite regelmäßig mit zusätzlichen Informationen über monogene Adipositas und andere seltene Erkrankungen des MC4R-Signalwegs.
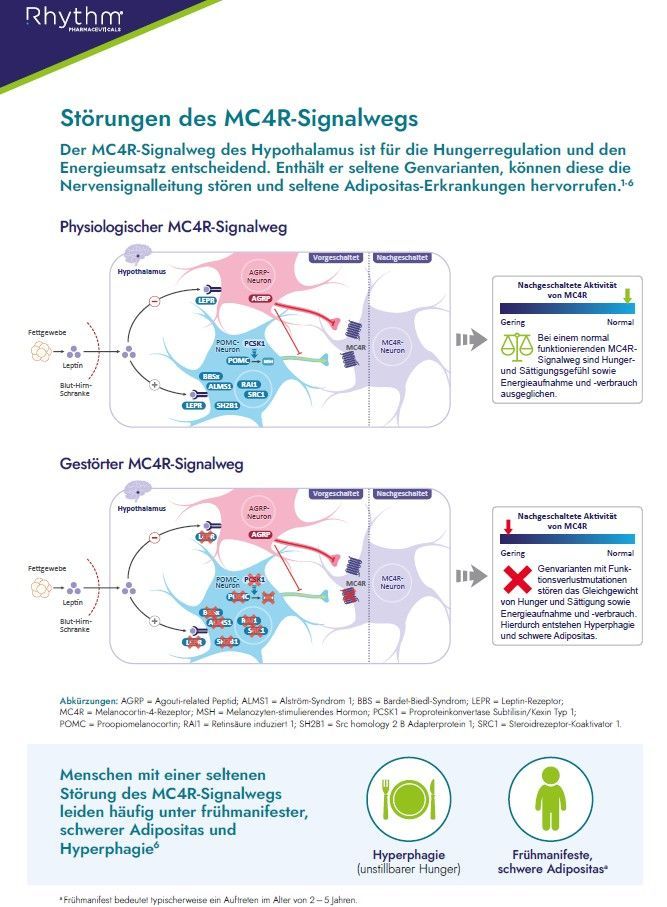
Störungen des MC4R-Signalwegs
Der MC4R-Signalweg des Hypothalamus ist für die Hungerregulation und den Energieumsatz entscheidend
Informationsblatt
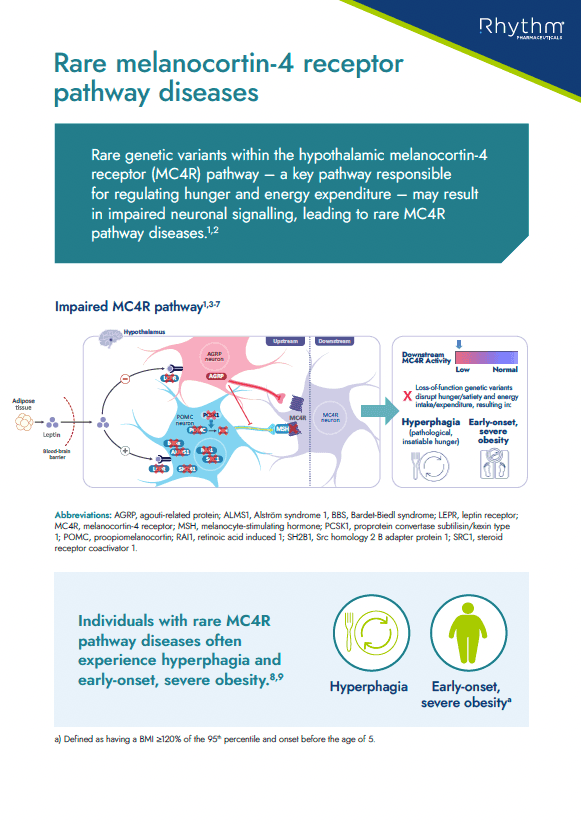
Educate HCPs on rare MC4R pathway diseases and how they can lead to hyperphagia and early-onset obesity
Informationsblatt
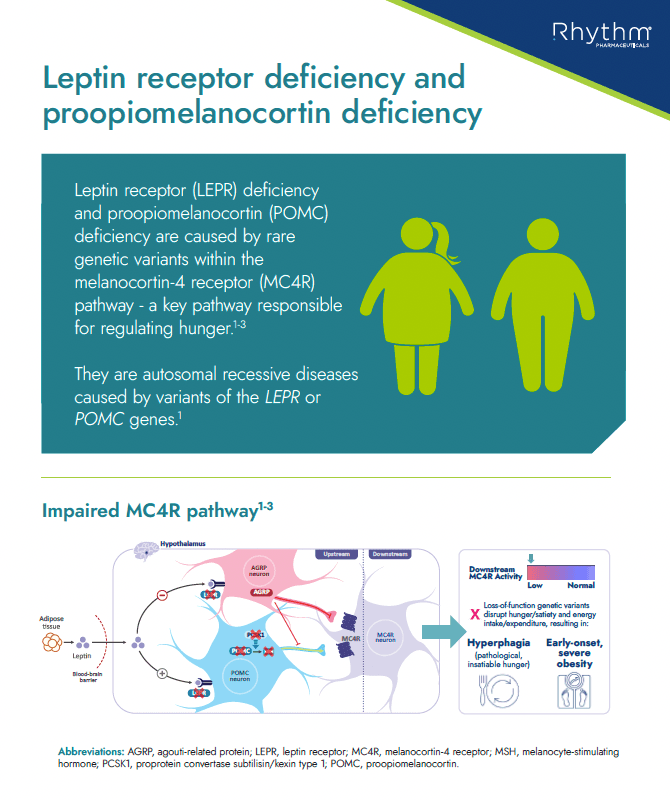
Schulungsmaterialien über LEPR- und POMC-Mangel (Worum handelt es sich? Was sind die wichtigsten Merkmale/klinischen Kennzeichen bei Patienten mit diesen Erkrankungen? Welche Prävalenz haben sie? Wie sieht der Weg zur Diagnose aus?)
Informationsblatt
Literatur:
- 1. Yazdi FT, et al. PeerJ. 2015;3:e856.
- 2. Acosta A, et al. Genes Nutr. 2014;9:384.
- 3. Haqq AM, et al. Lancet Diabetes Endocrinol. 2022;10(12):859–868.
- 4. Huvenne H, et al. Obes Facts. 2016;9:158–73
- 5. Fonseca ACP, et al. J Diabetes Complications. 2017;31:1549–1561.
- 6. Clément K, et al. Physiology Behavior. 2020;227:113134.
- 7. Styne DM, et al. J Clin Endocrinol Metab. 2017;102:709–757.
- 8. Heymsfield SB, et al. Obesity (Silver Spring). 2014;22:S1‒S17.
- 9. Ellacott KLJ & Cone RD. Philos Trans R Soc Lond B Biol Sci. 2006;361:1265–74.
- 10. Kohldorf K, et al. Int J Obes (Lond). 2018;42:1602–1609.
- 11. August GP, et al. J Clin Endocrinol Metab. 2008;93:4576–99.
- 12. Kleinendorst L, et al. BMJ Case Rep. 2017;2017:bcr2017221067.